Pendant des décennies, la réglementation des médicaments en vente libre (OTC) aux États-Unis est restée largement inchangée, s’appuyant sur un processus d’élaboration de règles lent et fastidieux. Cela a fondamentalement changé avec l’adoption de la loi CARES (Coronavirus Aid, Relief, and Economic Security Act) en 2020, qui a autorisé le Programme de frais d’utilisation des médicaments de monographie en vente libre (OMUFA).
Aujourd’hui, l’OMUFA n’est pas seulement un obstacle réglementaire ; il s’agit d’une exigence financière et opérationnelle essentielle pour toute entreprise fabriquant ou distribuant des médicaments monographiques en vente libre pour le marché américain. Le fait de ne pas comprendre la classification spécifique de votre établissement ou de ne pas respecter une échéance de frais limitée ne se limite pas à une amende mineure, cela peut conduire à ce que vos produits soient légalement considérés comme « mal étiquetés » et que votre entreprise soit placée sur la liste publique des arriérés de la FDA. Cette désignation publique arrête efficacement votre capacité à faire des affaires aux États-Unis, créant une paralysie opérationnelle qui peut prendre des mois à résoudre.
Le cœur de la réforme OTC : Pourquoi OMUFA existe-t-il ?
Avant l’OMUFA, le processus de la FDA pour la mise à jour des monographies de gré à gré était un cycle pluriannuel de « réglementation » qui avait du mal à suivre le rythme de l’innovation scientifique. OMUFA a remplacé cela par un processus de « commande administrative », conçu pour fournir à la FDA une source de revenus durable et financée par l’industrie pour :
- Moderniser le processus d’examen OTC : Passer des réglementations statiques à un système dynamique capable de répondre aux nouvelles données de sécurité en temps réel.
- Accélérer les délais scientifiques : Accélération de l’examen des nouveaux principes actifs, des formes galéniques et des indications précédemment langagées dans les carnets de commandes administratifs.
- Développer les ressources de l’agence : Financement du recrutement de réviseurs, chimistes et inspecteurs dédiés spécifiquement chargés de gérer le vaste et diversifié paysage des produits de monographie en vente libre.
En échange de ces frais, l’industrie pharmaceutique bénéficie d’un environnement réglementaire plus prévisible et plus efficace. Cependant, cette efficacité s’accompagne d’un strict mandat « pay-to-play » pour toutes les installations impliquées dans la chaîne d’approvisionnement.
Comprendre les types d’installations et les frais OMUFA
L’un des points de confusion les plus courants pour les fabricants est de déterminer quels frais s’appliquent à leur modèle commercial spécifique. Une mauvaise classification peut entraîner un trop-perçu important ou, à l’inverse, un trop-perçu qui déclenche un audit de conformité. La FDA classe les établissements en deux types principaux sous OMUFA :
1. Monographie de l’établissement pharmaceutique (MDF)
Un MDF est une installation étrangère ou nationale qui fabrique ou traite la « forme pharmaceutique finie » d’un médicament de monographie en vente libre. Cela inclut la forme physique finale du médicament, comme les comprimés, les gélules ou les crèmes topiques, destinée à un usage grand public.
- Qui paie : Toute installation qui fabrique, conditionne ou étiquette physiquement le produit final. Même si vous êtes un fabricant étranger expédiant à un distributeur américain, les frais MDF s’appliquent généralement à votre site de production.
- Le coût : Les MDF sont responsables de l’intégralité des frais annuels d’installation, qui sont ajustés chaque année pour répondre aux objectifs de revenus réglementaires de la FDA.
2. Monographie OTC Site de l’Organisation de fabrication sous contrat (CMO) de médicaments
Une installation de CMO est une installation qui fabrique la forme pharmaceutique finie d’un médicament de monographie en vente libre, mais qui n’est pas le propriétaire de cette installation de fabrication ni aucune filiale de ce propriétaire ou de cette installation ne vend le médicament de monographie en vente libre produit dans cette installation directement aux grossistes, détaillants ou consommateurs aux États-Unis.
- Qui paie : Généralement, les organisations de fabrication sous contrat entrent dans cette catégorie si elles produisent le médicament uniquement pour le compte d’un propriétaire de marque et ne tiennent pas la « commande » réglementaire pour le produit.
- Le coût : Pour tenir compte de leur rôle indirect dans le processus de demande de monographie, ces installations paient généralement des frais réduits, généralement fixés aux deux tiers des frais MDF standard.
Perspectives sur les frais 2025-2026
La FDA annonce annuellement les frais OMUFA, calculés en fonction de leurs coûts d’exploitation prévus, des ajustements de l’inflation et du nombre d’installations enregistrées dans le système. Étant donné que l’objectif de chiffre d’affaires total est fixé par la loi, les frais individuels par établissement peuvent fluctuer en fonction du nombre d’entreprises qui enregistrent et répertorient leurs produits avec succès chaque année.
| Type d’installation | Frais pour l’exercice 2024 | Frais pour l’exercice 2025 | Frais pour l’exercice 2026 |
| Monographie de l’établissement pharmaceutique (MDF) | 34 166 $ | 37 556 $ | 19 188 $ |
| Monographie OTC – Établissement CMO de médicaments | 22 777 $ | 25 037 $ | 12 792 $ |
Note : Les frais sont obligatoires et doivent être payés en totalité ; la FDA ne propose pas de frais ou de versements au prorata. Les chiffres finaux sont généralement publiés au Registre fédéral 45 jours avant la date limite de paiement.
Conséquences du non-paiement : La liste des arriérés de la FDA
Le risque le plus important et le plus immédiat de non-conformité à l’OMUFA est la liste des arriérés de la FDA. Si un établissement ne paie pas ses frais d’utilisateur requis dans les 20 jours suivant la date d’échéance, la FDA déplacera cet établissement de « en règle » à la liste publique des arriérés.
Implications profondes de la liste des arriérés :
- Fausse image de marque légale : Une fois répertoriés, tous les médicaments de monographie en vente libre fabriqués dans cet établissement sont légalement « mal étiquetés » en vertu de la Section 502(ff) de la Loi FD&C. Il est interdit d’introduire des médicaments mal étiquetés dans le commerce interétatique, exposant la société à des saisies et des injonctions.
- Alertes et détentions d’importation : Pour les établissements étrangers, le fait d’être sur la liste des arriérés est un signal d’alarme pour le Service des douanes et de la protection des frontières (CBP) des États-Unis. Les expéditions sont fréquemment retenues au port d’entrée, ce qui entraîne des produits avariés, des frais de surestaries et des chaînes d’approvisionnement rompues.
- Chute commerciale (risque du promoteur) : Les principaux détaillants (tels que Walmart, Target ou Amazon) et les distributeurs à grande échelle surveillent la liste des arriérés dans le cadre de la conformité standard de leurs fournisseurs. Si votre établissement y apparaît, vos partenaires peuvent être légalement contraints de retirer vos produits de leurs rayons afin d’éviter leur propre responsabilité pour la vente de produits mal étiquetés.
Navigation dans les OMOR : La voie de l’innovation
Au-delà des frais d’installation récurrents, OMUFA a introduit la demande de commande de monographie en vente libre (Over-the-Counter Monograph Order Request, OMOR). Il s’agit de la voie administrative officielle pour les entreprises cherchant à innover au sein du système de monographie, comme l’ajout d’un nouveau principe actif, la modification d’une limite de dosage ou la demande d’une nouvelle indication thérapeutique.
La FDA classe ces demandes en deux niveaux en fonction de la complexité de l’examen scientifique requis :
- Niveau 1 OMOR : Réservé aux demandes complexes et gourmandes en ressources. Cela comprend l’ajout d’un nouveau principe actif à une monographie, la création d’une toute nouvelle catégorie thérapeutique ou la modification de l’indication « standard » pour une classe entière de médicaments. Ces frais sont substantiels, dépassant actuellement 500 000 USD par demande, pour couvrir l’examen exhaustif des données cliniques requis.
- Niveau 2 OMOR : Couvre des changements plus ciblés et modestes. Il peut s’agir de réorganiser les avertissements de sécurité sur une étiquette, d’ajouter une forme posologique mineure qui ne nécessite pas de nouvelles études de sécurité clinique ou de clarifier les instructions d’utilisation spécifiques. Ces frais dépassent actuellement 100 000 USD par demande.
Principales échéances et mesures de conformité
La conformité OMUFA est un cycle de vie annuel qui nécessite une surveillance proactive. L’absence d’une seule fenêtre peut déclencher le processus Liste des arriérés. Pour rester en règle, votre équipe doit atteindre ces étapes spécifiques :
- Inscription annuelle et mise à jour de la liste : Vous devez vérifier et mettre à jour l’enregistrement de votre établissement et les listes de médicaments dans les portails de soumission officiels de la FDA. Si votre inscription est inexacte ou ne parvient pas à identifier correctement vos produits comme des médicaments de monographie, votre facture de frais sera incorrecte.
- Surveillance de l’annonce des frais : La FDA publie généralement les frais de l’exercice fiscal à venir dans le Registre fédéral. C’est le moment de sécuriser votre budget pour le paiement à venir.
- La fenêtre de paiement 45-Day : Une fois les frais annoncés, vous disposez d’une fenêtre très étroite, généralement de 45 jours, pour vous assurer que les fonds sont compensés par la banque de la FDA. Il est essentiel de surveiller de près ces délais changeants pour éviter d’être placé sur la liste des arriérés.
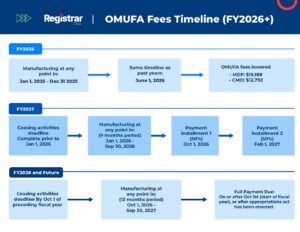
Voir cet organigramme OMUFA détaillé pour plus d’informations.
Comment Registrar Corp garantit votre conformité OMUFA
La gestion des frais d’utilisateur de la FDA implique plus que le traitement d’un simple paiement. Il nécessite une compréhension nuancée des classifications des installations et une détermination précise de la question de savoir si vos produits relèvent du système de « monographie » ou nécessitent une voie différente comme un NDA ou un ANDA.
Registrar Corp fournit un bouclier réglementaire complet pour s’assurer que votre activité OTC reste ininterrompue :
- Audit de classification des installations : Nous effectuons une analyse approfondie de vos opérations de fabrication pour nous assurer que vous êtes correctement classé. Nous avons aidé de nombreuses installations à éviter les paiements excessifs en les identifiant correctement comme des CMO plutôt que comme des MDF.
- Facilité de paiement sécurisée : Nous gérons le transfert électronique complexe des frais vers les comptes spécifiques de la FDA, en vous fournissant une preuve de paiement vérifiée qui peut être partagée avec les promoteurs et les courtiers en douane pour confirmer votre statut.
- Enregistrement et maintenance des listes : Nous gérons l’enregistrement annuel de votre établissement et les mises à jour de la liste des médicaments. Si les données internes de la FDA concernant vos produits de monographie ne correspondent pas parfaitement à l’enregistrement de votre établissement, cela peut entraîner des erreurs administratives qui compromettent votre position sur la liste des arriérés. Nous prévenons ces problèmes avant qu’ils ne se produisent.
- Intervention de crise (résolution des arriérés) : Si votre établissement figure déjà sur la liste des arriérés ou fait l’objet d’une détention à l’importation, nous fournissons une intervention immédiate pour régler les frais de retour, corriger les erreurs d’enregistrement et demander à la FDA de retirer de la liste pour rétablir votre accès au marché.
Protégez votre accès au marché américain et préservez la confiance de vos partenaires commerciaux. Contactez Registrar Corp dès aujourd’hui pour obtenir une assistance experte OMUFA de bout en bout.