几十年来,美国非处方药(OTC)的监管基本保持不变,依赖于缓慢,繁琐的规则制定过程。随着 2020 年冠状病毒援助、救济和经济安全 (CARES) 法案的通过,这一举措发生了根本性转变,该法案授权了非处方专论药物使用费计划 (OMUFA)。
如今,OMUFA 不仅仅是一个监管障碍;它是任何为美国市场制造或分销 OTC 专论药物的公司的关键财务和运营要求。不了解贵机构的具体分类或错过狭窄的收费截止日期不仅会导致轻微罚款,还可能导致您的产品在法律上被视为“错误品牌”,并且贵公司被列入公开的 FDA 警报名单。这一公开称号有效地阻止了您在美国开展业务的能力,造成了运营瘫痪,可能需要数月才能解决。
OTC 改革的核心:为什么 OMUFA 存在
在OMUFA之前,FDA更新OTC专论的过程是一个多年的“规则制定”周期,难以跟上科学创新的步伐。OMUFA 用“行政命令”流程取代了这一点,旨在为 FDA 提供可持续的、行业资助的收入来源,以:
- 现代化 OTC 审查流程:从静态法规转向可以实时响应新安全数据的动态系统。
- 加速科学时间表:加快审查以前在行政积压工作中枯竭的新活性成分、剂型和适应症。
- 扩展代理资源:为专门审查员、化学家和检查员的招聘提供资金,这些审查员、化学家和检查员专门负责管理场外专论产品的广阔和多样化。
作为这些费用的交换,制药行业获得了更可预测和更有效的监管环境。然而,这种效率对供应链中涉及的所有设施都具有严格的“付费”要求。
了解 OMUFA 设施类型和费用
制造商最常见的困惑点之一是确定哪些费用适用于他们的特定商业模式。分类错误可能导致严重超额付款,反之,导致低付款,从而触发合规审计。FDA 根据 OMUFA 将设施分为两类:
1. 专论药物设施 (MDF)
MDF 是制造或加工非处方药专论药物“成品剂型”的国外或国内设施。这包括供消费者使用的最终物理形式的药物,如片剂、胶囊或外用乳膏。
- 付款人:实际制造、包装或标记最终产品的任何设施。即使您是运送至美国分销商的外国制造商,MDF 费用通常也适用于您的生产场所。
- 成本:MDF 负责支付每年调整的设施年费,以达到 FDA 的法定收入目标。
2. OTC 专论药物合同制造组织 (CMO) 设施
CMO 设施是生产 OTC 专论药物成品剂型的设施,但不是此类制造设施的所有者,也不是此类所有者或设施的任何关联公司直接向美国的批发商、零售商或消费者销售此类设施生产的 OTC 专论药物。
- 付款人:通常,如果合同制造组织仅代表品牌所有者生产药物,并且不持有产品的监管“订单”,则属于此类别。
- 成本:为了说明他们在专著请求过程中的间接作用,这些设施通常支付降低的费用,通常设定为标准MDF费用的三分之二。
2025–2026 年费用展望
FDA 每年公布 OMUFA 费用,根据其预计运营成本、通货膨胀调整和系统中注册设施的数量计算。由于总收入目标由法律确定,因此每个设施的个人费用可能会根据每年成功注册和列出其产品的公司数量而波动。
| 设施类型 | 2024 财年费用 | 2025 财年费用 | 2026 财年费用 |
| 专论药物设施 (MDF) | 34,166 美元 | 37,556 美元 | 19,188 美元 |
| OTC 专论药物 CMO 设施 | 22,777 美元 | 25,037 美元 | 12,792 美元 |
注意:费用是强制性的,必须全额支付;FDA 不提供按比例分摊的费用或分期付款。最终数据通常在付款截止日期前 45 天发布在联邦登记簿中。
不付款的后果:FDA 欠款清单
OMUFA 不合规的最重要和最直接的风险是 FDA 申诉人名单。如果设施未能在到期日后 20 天内支付所需的用户费用,FDA 将把该设施从“信誉良好”转移到公共拖欠名单。
被列入追逐者名单的深远影响:
- 法律错误品牌:一旦上市,该机构生产的所有OTC专论药物均根据FD&C法案第502(ff)条合法“错误品牌”。禁止将错误品牌药物引入州际贸易,使公司面临扣押和禁令。
- 进口提醒和扣留:对于外国设施而言,列入领跑者名单是美国海关和边境保护局 (CBP) 的危险信号。货物经常在入境口岸被拘留,导致产品变质、滞期费和供应链中断。
- 商业影响(申办方风险):主要零售商(如沃尔玛、Target 或亚马逊)和大型分销商监控 Arrears List,作为其标准供应商合规的一部分。如果您的工厂出现,您的合作伙伴可能会被依法迫从货架上拿出您的产品,以避免他们自己对销售贴错品牌的商品负责。
OMOR 导航:创新之路
除了经常性设施费用外,OMUFA 还推出了非处方专论订单请求 (OMOR)。这是寻求在专著系统中进行创新的公司的官方行政途径,例如添加新的活性成分、更改剂量限制或请求新的治疗适应症。
FDA 根据所需科学审查的复杂性将这些请求分为两层:
- 一级 OMOR:保留用于复杂的资源密集型请求。这包括在专著中添加新的活性成分,创建一个全新的治疗类别,或更改整个药物类别的“标准”适应症。这些费用很高,目前每个请求超过 500,000 美元,以涵盖所需的详尽临床数据审查。
- 第 2 层 OMOR:涵盖更专注、更适度的变化。这可能包括重新排列标签上的安全性警告,添加不需要新的临床安全性研究的次要剂型,或澄清具体的使用说明。这些费用目前每次申请超过 100,000 美元。
关键截止日期和合规行动
OMUFA 合规性是一个需要主动监控的年度生命周期。缺少单个窗口可触发“拖欠列表”流程。为了保持良好的信誉,您的团队必须达到以下特定的里程碑:
- 年度注册和列表更新:您必须在 FDA 的官方提交门户中验证和更新您的机构注册和药物列表。如果您的注册不准确或未能正确地将您的产品标识为专论药物,您的费用发票将不正确。
- 费用公告监控:FDA 通常会在联邦登记簿中公布即将到来的财年费用。这是确保即将付款的预算的时刻。
- 45-Day付款窗口:一旦费用公布,你有一个非常窄的窗口 – 通常是45天 – 以确保资金由FDA的银行清算。密切关注这些不断变化的截止日期对于避免被列入拖欠名单至关重要。
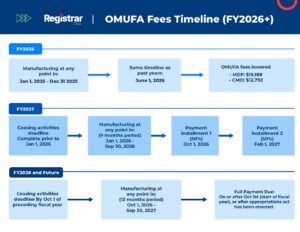
有关更多信息,请参见此详细的 OMUFA 流程图。
“注册商”如何确保您的 OMUFA 合规性
管理 FDA 用户费用不仅仅涉及处理付款。它需要对设施分类有细致的理解,并准确确定您的产品是否属于“单证”系统,或者是否需要像NDA或ANDA这样的不同途径。
Registrar Corp 提供全面的监管保护,确保您的场外交易业务不间断:
- 设施分类审计:我们对您的制造业务进行深入分析,以确保您被正确分类。我们帮助许多工厂避免了超额付款,将他们正确识别为 CMO,而不是 MDF。
- 安全支付便利:我们管理向 FDA 特定账户的复杂电子费用转移,为您提供经过验证的付款证明,可以与申办方和报关行共享,以确认您的状态。
- 注册和列表维护:我们管理您的年度设施注册和药物上市更新。如果 FDA 有关您专论产品的内部数据与您的设施注册不完全匹配,则可能导致管理错误,从而危及您在“拖欠名单”中的地位,我们会在这些问题发生之前予以预防。
- 危机干预 (Arrears Resolution):如果您的机构已经被列入拖欠名单或正面临进口拘留,我们会立即提供干预,以解决费用,纠正注册错误,并请求 FDA 从名单中删除以恢复您的市场准入。
保护您的美国市场准入,并维护您的商业合作伙伴的信心。立即联系 Registrar Corp 寻求专家级的端到端 OMUFA 协助。