Durante décadas, la regulación de los fármacos de venta sin receta (OTC) en los Estados Unidos se mantuvo prácticamente sin cambios, confiando en un proceso de elaboración de reglas lento y engorroso. Eso cambió fundamentalmente con la aprobación de la Ley de Ayuda, Alivio y Seguridad Económica del Coronavirus (CARES) en 2020, que autorizó el Programa de Honorarios de Usuario de Fármacos Monográficos de venta libre (OMUFA).
Hoy en día, OMUFA no es solo un obstáculo normativo; es un requisito financiero y operativo crítico para cualquier empresa que fabrica o distribuye fármacos monográficos OTC para el mercado estadounidense. No comprender la clasificación específica de su centro o no cumplir con un plazo de pago limitado no solo conlleva una multa menor, sino que puede hacer que sus productos se consideren legalmente “marcados incorrectamente” y que su empresa sea incluida en la lista pública de retrasos de la FDA. Esta designación pública detiene efectivamente su capacidad para hacer negocios en los Estados Unidos, creando una parálisis operativa que puede tardar meses en resolverse.
El núcleo de la reforma OTC: Por qué existe OMUFA
Antes de OMUFA, el proceso de la FDA para actualizar las monografías de OTC era un ciclo de “creación de reglas” de varios años que luchaba por mantener el ritmo de la innovación científica. OMUFA sustituyó esto por un proceso de “orden administrativa”, diseñado para proporcionar a la FDA un flujo de ingresos sostenible y financiado por la industria para:
- Modernizar el proceso de revisión de OTC: Alejándose de las regulaciones estáticas a un sistema dinámico que puede responder a nuevos datos de seguridad en tiempo real.
- Acelere los plazos científicos: Acelerar la revisión de nuevos ingredientes activos, formas de dosificación e indicaciones que anteriormente se langeaban en los atrasos administrativos.
- Expandir recursos de agencia: Financiar la contratación de revisores, químicos e inspectores dedicados específicamente encargados de gestionar el amplio y diverso panorama de los productos monográficos OTC.
A cambio de estas tarifas, la industria farmacéutica obtiene un entorno normativo más predecible y eficiente. Sin embargo, esta eficiencia viene con un estricto mandato de “pago por juego” para todas las instalaciones involucradas en la cadena de suministro.
Comprensión de los tipos y tarifas de las instalaciones de OMUFA
Uno de los puntos de confusión más comunes para los fabricantes es determinar qué tarifa se aplica a su modelo de negocio específico. Una clasificación errónea puede dar lugar a un pago excesivo o, por el contrario, a un pago insuficiente que desencadene una auditoría de cumplimiento. La FDA clasifica las instalaciones en dos tipos principales bajo OMUFA:
1. Monografía del centro de medicamentos (MDF)
Un MDF es una instalación extranjera o nacional que fabrica o procesa la “forma de dosificación terminada” de un fármaco monográfico OTC. Esto incluye la forma física final del fármaco, como comprimidos, cápsulas o cremas tópicas, destinadas al uso del consumidor.
- Quién paga: Cualquier instalación que fabrique, empaquete o etiquete físicamente el producto final. Incluso si usted es un fabricante extranjero que envía a un distribuidor de EE. UU., la tarifa MDF generalmente se aplica a su centro de producción.
- El coste: Los MDF son responsables de la tarifa anual completa de las instalaciones, que se ajusta anualmente para cumplir con los objetivos de ingresos legales de la FDA.
2. Monografía OTC Organización de fabricación contratada de fármacos (CMO) Instalación
Una instalación de CMO es una instalación que fabrica la forma de dosificación terminada de un fármaco monográfico OTC pero no es el propietario de dicha instalación de fabricación ni ninguna filial de dicho propietario o instalación vende el fármaco monográfico OTC producido en dicha instalación directamente a mayoristas, minoristas o consumidores en los Estados Unidos.
- Quién paga: Normalmente, las organizaciones de fabricación por contrato entran en esta categoría si están produciendo el fármaco únicamente en nombre de un propietario de marca y no tienen el “pedido” reglamentario para el producto.
- El coste: Para tener en cuenta su papel indirecto en el proceso de solicitud de monografía, estas instalaciones generalmente pagan una tarifa reducida, normalmente establecida en dos tercios de la tarifa estándar del MDF.
Perspectivas de la cuota para 2025-2026
La FDA anuncia los honorarios de OMUFA anualmente, calculados en función de sus costes operativos previstos, ajustes de inflación y el número de instalaciones registradas en el sistema. Debido a que el objetivo de ingresos totales es fijo por ley, la tarifa individual por instalación puede fluctuar dependiendo de cuántas empresas registren y enumeren sus productos con éxito cada año.
| Tipo de instalación | Cargo del año fiscal 2024 | Cargo del año fiscal 2025 | Cargo del año fiscal 2026 |
| Monografía del centro de medicamentos (MDF) | $34,166 | $37,556 | $19,188 |
| Centro de CMO de fármacos monográficos OTC | $22,777 | $25,037 | $12,792 |
Nota: Las tarifas son obligatorias y deben pagarse en su totalidad; la FDA no ofrece tarifas prorrateadas ni cuotas. Las cifras finales suelen publicarse en el Registro Federal 45 días antes de la fecha límite de pago.
Las consecuencias de la falta de pago: La lista de la FDA llega
El riesgo más significativo e inmediato de incumplimiento de OMUFA es la lista de retrasos de la FDA. Si una instalación no paga la tarifa de usuario requerida en un plazo de 20 días a partir de la fecha de vencimiento, la FDA trasladará esa instalación de “al día” a la Lista pública de moras.
Implicaciones profundas de estar en la lista de atrasos:
- Errores legales de marca: Una vez enumerados, todos los fármacos monográficos OTC fabricados en esa instalación están legalmente “marcados incorrectamente” en virtud de la Sección 502(ff) de la Ley FD&C. Es un acto prohibido introducir fármacos de marca incorrecta en el comercio interestatal, exponiendo a la empresa a incautaciones y medidas cautelares.
- Detenciones y alertas de importación: Para las instalaciones extranjeras, estar en la Lista de atrasos es una señal de alerta para la Oficina de Aduanas y Protección Fronteriza (Customs and Border Protection, CBP) de los EE. UU. Los envíos se detienen con frecuencia en el puerto de entrada, lo que da lugar a productos estropeados, tasas de demora y cadenas de suministro rotas.
- Cataratas comerciales (riesgo del promotor): Los principales minoristas (como Walmart, Target o Amazon) y los distribuidores a gran escala supervisan la Lista de atrasos como parte del cumplimiento de sus proveedores estándar. Si su instalación aparece allí, sus socios pueden verse obligados legalmente a sacar sus productos de sus estantes para evitar su propia responsabilidad por la venta de productos con una marca incorrecta.
Navegación por los OMOR: El camino de la innovación
Más allá de las tarifas recurrentes de las instalaciones, OMUFA presentó la Solicitud de pedido de monografía de venta libre (OMOR). Esta es la vía administrativa oficial para las empresas que buscan innovar dentro del sistema monográfico, como añadir un nuevo ingrediente activo, cambiar un límite de dosis o solicitar una nueva indicación terapéutica.
La FDA clasifica estas solicitudes en dos niveles en función de la complejidad de la revisión científica requerida:
- OMOR de nivel 1: Reservado para solicitudes complejas que consumen muchos recursos. Esto incluye añadir un nuevo ingrediente activo a una monografía, crear una nueva categoría terapéutica o cambiar la indicación “estándar” para toda una clase de fármacos. Estos honorarios son sustanciales, actualmente superan los 500 000 USD por solicitud, para cubrir la revisión exhaustiva de los datos clínicos requerida.
- OMOR de nivel 2: Cubre cambios más centrados y modestos. Esto podría incluir volver a ordenar las advertencias de seguridad en una etiqueta, añadir una forma de dosificación menor que no requiera nuevos estudios de seguridad clínica o aclarar instrucciones de uso específicas. Estos cargos actualmente superan los $100,000 por solicitud.
Plazos clave y acciones de cumplimiento
El cumplimiento de OMUFA es un ciclo de vida anual que requiere supervisión proactiva. Si falta una sola ventana, se puede activar el proceso de lista de atrasos. Para mantenerse al día, su equipo debe alcanzar estos hitos específicos:
- Actualización de registro anual y listado: Debe verificar y actualizar el registro de su centro y los listados de fármacos en los portales de envío oficiales de la FDA. Si su registro es inexacto o no identifica correctamente sus productos como fármacos monográficos, su factura de honorarios será incorrecta.
- Monitoreo de anuncio de tarifa: La FDA normalmente publica los honorarios del próximo año fiscal en el Registro Federal. Este es el momento de asegurar su presupuesto para el próximo pago.
- El plazo de pago 45-Day: Una vez que se anuncian los cargos, tiene un margen muy estrecho, normalmente de 45 días, para garantizar que los fondos sean autorizados por el banco de la FDA. Es esencial estar atento a estos plazos cambiantes para evitar ser incluido en la Lista de atrasos.
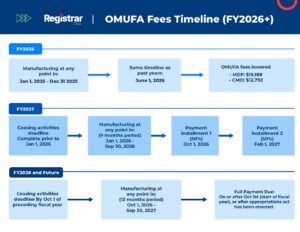
Consulte este diagrama de flujo OMUFA detallado para obtener más información.
Cómo Registrar Corp garantiza su cumplimiento de OMUFA
La gestión de las tarifas de usuario de la FDA implica algo más que procesar un pago. Requiere una comprensión matizada de las clasificaciones de las instalaciones y una determinación precisa de si sus productos entran dentro del sistema monográfico o requieren una ruta diferente como un NDA o ANDA.
Registrar Corp proporciona un escudo normativo integral para garantizar que su negocio de OTC permanezca ininterrumpido:
- Auditoría de clasificación de instalaciones: Llevamos a cabo un análisis exhaustivo de sus operaciones de fabricación para garantizar que se clasifique correctamente. Hemos ayudado a numerosas instalaciones a evitar el pago excesivo al identificarlas correctamente como CMO en lugar de MDF.
- Facilitación de pagos seguros: Gestionamos la compleja transferencia electrónica de tarifas a cuentas específicas de la FDA, proporcionándole una prueba de pago verificada que puede compartirse con patrocinadores y agentes de aduanas para confirmar su estado.
- Mantenimiento de registro y listado: Gestionamos el registro anual de su centro y las actualizaciones de la lista de medicamentos. Si los datos internos de la FDA relativos a sus productos monográficos no coinciden perfectamente con el registro de su centro, pueden provocar errores administrativos que pongan en peligro su posición en la Lista de moras: evitamos estos problemas antes de que ocurran.
- Intervención de crisis (resolución de atrasos): Si su centro ya está en la lista de retrasos o se enfrenta a una detención de importación, le proporcionamos una intervención inmediata para liquidar las tarifas, corregir los errores de registro y solicitar a la FDA que la elimine de la lista para restaurar su acceso al mercado.
Proteja su acceso al mercado de EE. UU. y mantenga la confianza de sus socios comerciales. Póngase en contacto con Registrar Corp hoy mismo para obtener asistencia OMUFA integral y experta.