Per decenni, la regolamentazione dei farmaci da banco (OTC) negli Stati Uniti è rimasta in gran parte invariata, basandosi su un lento e ingombrante processo di regolamentazione. Ciò è cambiato radicalmente con l’approvazione del Coronavirus Aid, Relief, and Economic Security Act (CARES) nel 2020, che ha autorizzato l’Over-the-Counter Monograph Drug User Fee Program (OMUFA).
Oggi, OMUFA non è solo un ostacolo normativo; è un requisito finanziario e operativo fondamentale per qualsiasi azienda che produce o distribuisce farmaci monografici OTC per il mercato statunitense. La mancata comprensione della classificazione specifica della tua struttura o la mancata scadenza di una tassa ristretta non si traducono solo in una multa minore: può portare ai tuoi prodotti a essere legalmente considerati “marcheggiati erroneamente” e alla tua azienda essere inserita nell’elenco pubblico di Arrears della FDA. Questa designazione pubblica blocca efficacemente la tua capacità di fare affari negli Stati Uniti, creando una paralisi operativa che può richiedere mesi per risolversi.
Il nucleo della riforma OTC: Perché esiste l’OMUFA
Prima dell’OMUFA, il processo della FDA per l’aggiornamento delle monografie OTC era un ciclo pluriennale di “regolemaking” che faticava a tenere il passo con l’innovazione scientifica. OMUFA ha sostituito questo con un processo di “ordine amministrativo”, progettato per fornire alla FDA un flusso di entrate sostenibile e finanziato dall’industria per:
- Modernizzare il processo di revisione OTC: Passando dalle normative statiche a un sistema dinamico in grado di rispondere ai nuovi dati di sicurezza in tempo reale.
- Accelera le tempistiche scientifiche: Accelerare la revisione di nuovi principi attivi, forme di dosaggio e indicazioni che in precedenza languivano in arretrati amministrativi.
- Espandere le risorse dell’agenzia: Finanziare l’assunzione di revisori, chimici e ispettori dedicati specificamente incaricati di gestire il vasto e diversificato panorama dei prodotti monografici OTC.
In cambio di queste tasse, l’industria farmaceutica guadagna un ambiente normativo più prevedibile ed efficiente. Tuttavia, questa efficienza viene fornita con un rigoroso mandato “pay-to-play” per tutte le strutture coinvolte nella catena di approvvigionamento.
Comprensione dei tipi e delle tariffe delle strutture OMUFA
Uno dei punti di confusione più comuni per i produttori è determinare quale tassa si applica al loro modello di business specifico. La classificazione errata può portare a un pagamento in eccesso significativo o, al contrario, a un pagamento inadeguato che innesca un audit di conformità. La FDA categorizza le strutture in due tipi principali sotto OMUFA:
1. Struttura farmaceutica per monografie (MDF)
Un MDF è una struttura straniera o nazionale che produce o elabora la “forma di dosaggio finito” di un farmaco monografico OTC. Ciò include la forma fisica finale del farmaco, come compresse, capsule o creme topiche, destinate all’uso da parte dei consumatori.
- Chi paga: Qualsiasi struttura che produce, imballa o etichetta fisicamente il prodotto finale. Anche se sei un produttore straniero che spedisce a un distributore statunitense, la tariffa MDF si applica generalmente al tuo sito di produzione.
- Il costo: Gli MDF sono responsabili dell’intera tassa annuale della struttura, che viene regolata annualmente per soddisfare gli obiettivi di entrate legali della FDA.
2. Stabilimento dell’Organizzazione per la produzione di contratti farmacologici (CMO) per monografie OTC
Una struttura CMO è una struttura che produce la forma di dosaggio finale di un farmaco monografico OTC, ma non è proprietaria di tale impianto di produzione né alcuna affiliata di tale proprietario o impianto vende il farmaco monografico OTC prodotto in tale stabilimento direttamente a grossisti, rivenditori o consumatori negli Stati Uniti.
- Chi paga: In genere, le organizzazioni di produzione a contratto rientrano in questa categoria se stanno producendo il farmaco esclusivamente per conto di un proprietario del marchio e non detengono l'”ordine” normativo per il prodotto.
- Il costo: Per tenere conto del loro ruolo indiretto nel processo di richiesta di monografia, queste strutture generalmente pagano una commissione ridotta, in genere fissata a due terzi della tariffa MDF standard.
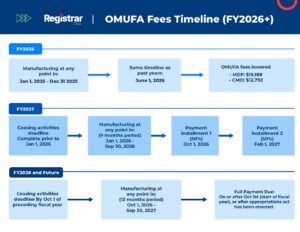
Prospettive sulle commissioni 2025-2026
La FDA annuncia annualmente le tariffe OMUFA, calcolate in base ai costi operativi previsti, agli adeguamenti dell’inflazione e al numero di strutture registrate nel sistema. Poiché l’obiettivo di fatturato totale è fissato dalla legge, la tariffa individuale per struttura può variare a seconda di quante aziende registrano ed elencano con successo i loro prodotti ogni anno.
| Tipo di struttura | Commissione per l’anno fiscale 2024 | Commissione per l’anno fiscale 2025 | Commissione per l’anno fiscale 2026 |
| Struttura farmaceutica per monografie (MDF) | 34.166 USD | 37.556 USD | 19.188 USD |
| Struttura OTC Monograph Drug CMO | 22.777 USD | 25.037 USD | 12.792 USD |
Nota: Le tariffe sono obbligatorie e devono essere pagate per intero; la FDA non offre tariffe o rate proporzionate. Le cifre finali sono solitamente pubblicate nel Registro federale 45 giorni prima della scadenza del pagamento.
Le conseguenze del mancato pagamento: La lista degli Arrears della FDA
Il rischio più significativo e immediato di non conformità OMUFA è la FDA Arrears List. Se una struttura non riesce a pagare la tassa utente richiesta entro 20 giorni dalla data di scadenza, la FDA trasferirà tale struttura da “buona reputazione” alla pubblica lista Arrears.
Implicazioni profonde dell’essere nella lista Arrears:
- Errore di branding legale: Una volta elencati, tutti i farmaci monografici da banco fabbricati presso tale struttura sono legalmente “contrassegnati” ai sensi della Sezione 502(ff) del FD & C Act. È un atto vietato introdurre farmaci contraffatti nel commercio interstatale, esponendo l’azienda a sequestri e ingiunzioni.
- Avvisi di importazione e detenzioni: Per le strutture straniere, essere nella lista Arrears è una bandiera rossa per la protezione doganale e delle frontiere degli Stati Uniti (CBP). Le spedizioni vengono spesso trattenute nel porto di entrata, portando a prodotti rovinati, commissioni di demurrage e catene di approvvigionamento rotte.
- Fallout commerciale (rischio dello sponsor): I principali rivenditori (come Walmart, Target o Amazon) e i distributori su larga scala monitorano l’elenco Arrears come parte della conformità standard dei fornitori. Se la tua struttura appare lì, i tuoi partner potrebbero essere legalmente costretti a ritirare i tuoi prodotti dai loro scaffali per evitare la propria responsabilità per la vendita di merci con marchio errato.
Navigazione negli OMOR: Il percorso dell’innovazione
Oltre alle spese ricorrenti per la struttura, OMUFA ha introdotto la richiesta di ordine di monografie over-the-counter (OMOR). Questo è il percorso amministrativo ufficiale per le aziende che cercano di innovare all’interno del sistema monografico, come l’aggiunta di un nuovo principio attivo, la modifica di un limite di dosaggio o la richiesta di una nuova indicazione terapeutica.
La FDA classifica queste richieste in due livelli in base alla complessità della revisione scientifica richiesta:
- OMOR di livello 1: Riservato per richieste complesse e ad alta intensità di risorse. Ciò include l’aggiunta di un nuovo principio attivo a una monografia, la creazione di una nuova categoria terapeutica o la modifica dell’indicazione “standard” per un’intera classe di farmaci. Queste tariffe sono sostanziali, attualmente superiori a $ 500.000 per richiesta, per coprire l’esauriente revisione dei dati clinici richiesti.
- OMOR di livello 2: Copre cambiamenti più mirati e modesti. Ciò potrebbe includere il riordino delle avvertenze di sicurezza su un’etichetta, l’aggiunta di una forma di dosaggio minore che non richiede nuovi studi clinici sulla sicurezza o il chiarimento di istruzioni d’uso specifiche. Queste commissioni attualmente superano i 100.000 USD per richiesta.
Scadenze principali e azioni di conformità
La conformità OMUFA è un ciclo di vita annuale che richiede un monitoraggio proattivo. La mancanza di una singola finestra può attivare il processo Elenco Arrears. Per mantenere una buona reputazione, il tuo team deve raggiungere questi traguardi specifici:
- Aggiornamento annuale della registrazione e dell’elenco: È necessario verificare e aggiornare la registrazione della struttura e gli elenchi dei farmaci nei portali di presentazione ufficiali della FDA. Se la registrazione non è accurata o non riesce a identificare correttamente i prodotti come farmaci monografici, la fattura della tariffa non sarà corretta.
- Monitoraggio dell’annuncio delle commissioni: La FDA pubblica in genere le tasse dell’anno fiscale imminente nel Registro federale. Questo è il momento di garantire il tuo budget per il pagamento imminente.
- Finestra di pagamento di 45-Day: Una volta che le tasse sono annunciate, si dispone di una finestra molto stretta, in genere 45 giorni, per garantire che i fondi siano liquidati dalla banca della FDA. Tenere sotto stretta osservazione queste scadenze in continuo cambiamento è essenziale per evitare di essere inseriti nella lista Arrears.
Per ulteriori informazioni, vedere questo diagramma di flusso OMUFA dettagliato.
Come Registrar Corp garantisce la conformità OMUFA
La gestione delle tariffe degli utenti della FDA comporta molto di più della semplice elaborazione di un pagamento. Richiede una comprensione sfumata delle classificazioni delle strutture e una determinazione precisa del fatto che i tuoi prodotti rientrino nel sistema “monografico” o richiedano un percorso diverso come un NDA o un ANDA.
Registrar Corp fornisce uno scudo normativo completo per garantire che la tua attività OTC rimanga ininterrotta:
- Verifica della classificazione della struttura: Conduciamo un’analisi approfondita delle vostre operazioni di produzione per assicurarci che siate classificati correttamente. Abbiamo aiutato numerose strutture a evitare il pagamento eccessivo identificandole correttamente come CMO anziché MDF.
- Facilitazione del pagamento sicuro: Gestiamo il complesso trasferimento elettronico delle tasse ai conti specifici della FDA, fornendovi una prova di pagamento verificata che può essere condivisa con sponsor e broker doganali per confermare il vostro stato.
- Registrazione e manutenzione degli elenchi: Gestiamo la registrazione annuale della struttura e gli aggiornamenti dell’elenco dei farmaci. Se i dati interni della FDA riguardanti i tuoi prodotti monografici non corrispondono perfettamente alla registrazione della tua struttura, possono portare a errori amministrativi che mettono a rischio la tua posizione nella lista Arrears: preveniamo questi problemi prima che si verifichino.
- Intervento di crisi (risoluzione irregolare): Se la tua struttura è già nell’elenco Arrears o sta affrontando una detenzione per l’importazione, forniamo un intervento immediato per risolvere le tasse, correggere gli errori di registrazione e chiedere alla FDA la rimozione dall’elenco per ripristinare l’accesso al mercato.
Proteggi il tuo accesso al mercato statunitense e mantieni la fiducia dei tuoi partner commerciali. Contattate oggi stesso Registrar Corp per ricevere assistenza OMUFA end-to-end.