¿Necesito la aprobación de la FDA? Lograr el cumplimiento de la FDA con Registrar Corp
Aprender a obtener la aprobación de la FDA, o determinar si incluso la necesita, depende completamente del tipo de producto que planea comercializar en los EE. UU. Muchos asumen que todos los productos deben revisarse y aprobarse antes de entrar en el mercado, pero la realidad es mucho más matizada. La FDA no requiere que todos los productos sean aprobados antes de entrar en el mercado y, en algunos casos, solo ciertos componentes, como ingredientes específicos, deben someterse al proceso. Un malentendido de estas distinciones puede conducir a costosos retrasos, infracciones de etiquetado e incluso acciones de aplicación.
Para tomar decisiones informadas, las empresas necesitan algo más que definiciones: deben comprender las vías regulatorias, las apuestas de incumplimiento y las consecuencias de actuar sobre mitos. Esta guía explica cada categoría de producto principal que la FDA regula, explicando cuándo se requiere aprobación, cuándo no y qué pasos de cumplimiento siguen siendo aplicables. También aborda conceptos erróneos comunes, proporciona un gráfico de referencia rápida y enlaces a recursos autorizados de la FDA. En todo momento, una verdad fundamental es: El registro de la FDA no es lo mismo que la aprobación de la FDA, y suponer que de otro modo puede ser un error costoso.
Referencia rápida: Requisitos de aprobación y registro de la FDA
| Categoría | ¿Se requiere aprobación de la FDA? | ¿Se requiere registro? | Excepciones clave |
| Alimentos y bebidas | No | Sí (la mayoría de las instalaciones) | Nuevos aditivos alimentarios |
| Suplementos alimenticios | No | Sí (la mayoría de las instalaciones) | Las afirmaciones sobre enfermedades desencadenan la regulación de los fármacos |
| Medicamentos | A veces | Sí | Las monografías OTC que cumplen con las normas no requieren aprobación |
| Dispositivos médicos | Solo clase III | Sí | Ciertas Clases I y II requieren espacio libre 510(k) |
| Cosméticos | No (excepto aditivos de color) | Sí (en MoCRA) | Las afirmaciones que afectan a la estructura/función pueden desencadenar regulaciones de fármacos |
| Aditivos de color | Sí | N/P | Algunos requieren certificación por lotes |
Aprobación de alimentos, bebidas y suplementos dietéticos por parte de la FDA
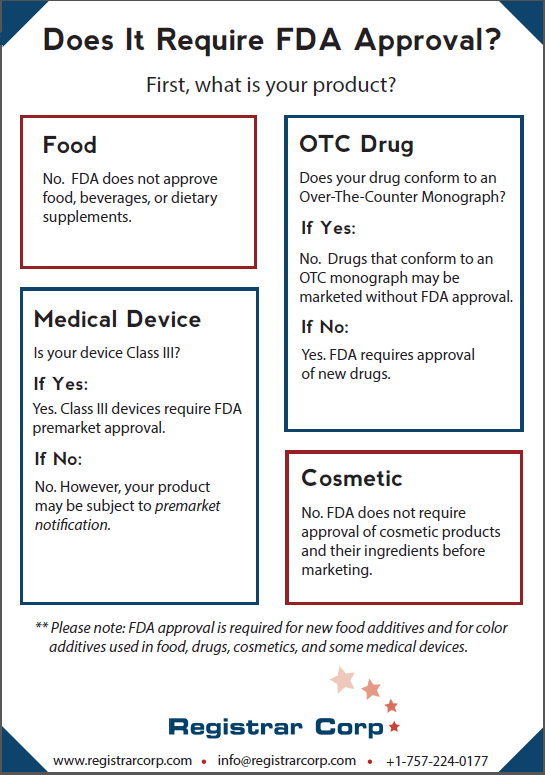
A diferencia de la creencia popular, la FDA no aprueba alimentos, bebidas o suplementos dietéticos antes de que se vendan en los Estados Unidos. Las instalaciones alimentarias no necesitan certificación ni aprobación previa a la comercialización, pero la mayoría debe registrarse en la FDA y cumplir con la Ley de Modernización de la Seguridad Alimentaria (FSMA).
El registro tiene dos propósitos principales: proporciona a la FDA la información de contacto necesaria para las comunicaciones rutinarias y de emergencia, e informa a la agencia sobre los productos y actividades en la instalación. Esta información permite a la FDA establecer prioridades de inspección basadas en posibles riesgos para la seguridad alimentaria, centrándose en las operaciones de mayor riesgo mientras se siguen realizando comprobaciones aleatorias. Por ejemplo, una instalación que produce alimentos listos para comer puede inspeccionarse con más frecuencia que un procesador de productos básicos de bajo riesgo.
La FDA hace cumplir estos requisitos mediante la inspección de las instalaciones registradas, la emisión de cartas de advertencia por infracciones y la detención de envíos que parezcan no conformes. El registro también permite la difusión específica durante retiradas o emergencias de salud pública. Sin embargo, aunque se requiere el registro para la mayoría de las instalaciones de alimentos y suplementos, no debe confundirse con la aprobación del producto. Esta distinción es fundamental en todos los sectores regulados por la FDA.
Además, la FSMA exige que las instalaciones implementen y mantengan un plan de seguridad alimentaria supervisado por una persona calificada para controles preventivos (PCQI). Completar un programa de capacitación PCQI reconocido ayuda a garantizar que la persona responsable esté equipada para identificar peligros, validar controles y gestionar el cumplimiento. Sin un PCQI designado, las empresas se arriesgan a tomar medidas de aplicación y a demoras en la resolución de los hallazgos de la inspección.
Una de las pocas excepciones en esta categoría son los aditivos alimentarios. A menos que se reconozca generalmente como seguro (GRAS), cualquier aditivo nuevo debe aprobarse a través de una petición de aditivo alimentario, que requiere pruebas rigurosas y datos de seguridad en virtud de la Ley de FD&C.
El uso previsto es importante: cuando un producto cruza la línea de la nutrición a las afirmaciones terapéuticas, puede entrar en una nueva categoría reguladora por completo, una que requiere aprobación. Por ejemplo, los suplementos dietéticos que afirman tratar, diagnosticar, prevenir o curar enfermedades pueden regularse como fármacos y luego estarían sujetos al proceso de aprobación descrito en la siguiente sección.
Destruir el mito: Los alimentos “aprobados por la FDA” no existen. Incluso si una instalación está registrada y cumple plenamente con las normas, ni la instalación ni sus productos han sido aprobados oficialmente a menos que ingredientes específicos, como aditivos, hayan pasado por el proceso de aprobación.
Aprobación de medicamentos por parte de la FDA: Cómo obtener la aprobación de la FDA
El hecho de que un nuevo fármaco requiera la aprobación de la FDA depende de si se ajusta a una monografía de venta sin receta (OTC). Las monografías OTC detallan las condiciones específicas en las que un fármaco se considera seguro y eficaz sin aprobación previa a la comercialización. Las monografías finales funcionan como “recetas” para las categorías de fármacos, especificando los ingredientes, las dosis, el etiquetado y las normas de prueba. La FDA también ejerce la discreción de aplicación para ciertos fármacos en virtud de monografías finales provisionales.
Si un fármaco no cumple con una monografía de OTC, debe someterse a la aprobación previa a la comercialización. Este proceso implica análisis de laboratorio, estudios en animales y ensayos clínicos en seres humanos por fases, seguidos de la presentación de datos a la FDA. La agencia revisa los datos para determinar si los beneficios superan los riesgos del uso previsto. La comercialización de un fármaco no conforme sin aprobación está prohibida en virtud de la Ley de Alimentos, Medicamentos y Cosméticos (FD&C Act). La FDA no aprueba los fármacos compuestos.
Los establecimientos de fármacos deben registrar y enumerar sus productos ante la FDA para supervisar a la agencia para la inspección y el control del cumplimiento. De nuevo, este proceso de registro y listado, si bien es necesario, no implica que la FDA haya aprobado el fármaco o el establecimiento.
Al igual que los fármacos, los dispositivos médicos siguen un camino escalonado hacia el mercado, aunque los criterios y umbrales de aprobación difieren.
Destruir el mito: Muchos creen que la FDA debe aprobar todos los fármacos antes de su comercialización. En realidad, si un fármaco cumple con una monografía OTC, puede comercializarse legalmente sin aprobación previa a la comercialización.
Aprobación de dispositivos médicos por parte de la FDA: Cómo obtener la aprobación de la FDA para productos de clase III
La FDA clasifica los dispositivos médicos en tres categorías según el riesgo: Clase I (riesgo bajo), Clase II (riesgo moderado) y Clase III (riesgo alto). Los dispositivos de clase III, como marcapasos o ciertos implantes, requieren aprobación previa a la comercialización, que exige pruebas sólidas de seguridad y eficacia a través de ensayos clínicos y documentación técnica.
Los dispositivos de clase I y II, a menos que estén exentos, deben presentar una notificación previa a la comercialización (510(k)) que demuestre una equivalencia sustancial con un dispositivo comercializado legalmente. Esto implica proporcionar especificaciones detalladas del producto, datos de rendimiento y, a veces, evidencia clínica. Si la FDA determina la equivalencia, “autoriza” el dispositivo para su comercialización en lugar de “aprobarlo”. Al igual que con otras categorías, los requisitos de registro y listado de dispositivos ayudan a la FDA a supervisar la actividad del sector, pero no equivalen a la aprobación del producto.
Destruir el mito: “Autorizado por la FDA” y “autorizado por la FDA” no son intercambiables. De los sujetos a la revisión de la FDA, la mayoría de los dispositivos se autorizan a través del proceso 510(k), no se aprueban. Solo los dispositivos de clase III requieren una aprobación previa a la comercialización completa.
Aprobación de cosméticos por parte de la FDA
La FDA no requiere que los productos cosméticos o sus ingredientes sean aprobados antes de su comercialización, excepto los aditivos de color. Antes de diciembre de 2022, las empresas de cosméticos no tenían que registrarse en absoluto en la FDA. En virtud de la Ley de Modernización de Regulaciones Cosméticas (Modernization of Cosmetic Regulations Act, MoCRA), las empresas ahora deben registrar sus instalaciones y enumerar sus productos.
Antes de MoCRA, la supervisión de la FDA dependía en gran medida de la aplicación posterior a la comercialización, interviniendo cuando los productos se encontraban inseguros o con una marca errónea. Ahora, con el registro obligatorio, la FDA tiene una mejor visibilidad, puede evaluar el cumplimiento de forma proactiva y programar inspecciones basadas en perfiles de riesgo.
Es importante tener en cuenta que el registro no es lo mismo que la aprobación. La idea errónea persiste en que el registro de la FDA indica la aprobación de un producto, cuando de hecho simplemente otorga a la FDA la autoridad para inspeccionar y supervisar el cumplimiento. Además, las afirmaciones cosméticas que implican beneficios terapéuticos, como curar o prevenir enfermedades, pueden hacer que la FDA regule el producto como fármaco, lo que puede requerir aprobación.
Ahondar en el mito: El registro cosmético bajo MoCRA no significa que la FDA haya aprobado el producto. La aprobación solo se aplica a aditivos de color específicos o si el producto está regulado como fármaco.
Una excepción clave a este modelo no aprobado son los aditivos de color, ya sean utilizados en cosméticos, alimentos o fármacos, que están regulados bajo su propio proceso de aprobación.
Aprobación de aditivos de color por parte de la FDA
La FDA debe aprobar los aditivos de color utilizados en alimentos, fármacos, cosméticos y ciertos dispositivos médicos. Esta aprobación garantiza que el aditivo cumpla con las normas de seguridad para su uso previsto. Ciertos colores de alto riesgo requieren certificación por lotes para cada lote antes de su uso.
Los aditivos de color solo se pueden utilizar de acuerdo con sus especificaciones y restricciones aprobadas. Los productos que contienen aditivos de color no aprobados se consideran adulterados según la Ley de FD&C y pueden detenerse en los puertos de entrada de EE. UU.
Ahondar en el mito: La aprobación de un aditivo de color para un uso no permite su uso en otras categorías de productos. Cada uso aprobado tiene limitaciones y condiciones específicas.
Etiquetado de productos aprobados por la FDA
Incluso para los productos aprobados, hay otra área que desafía a los fabricantes: el etiquetado. Los fabricantes de fármacos y dispositivos que requieren aprobación pueden incluir “Aprobado por la FDA” en la etiqueta del producto si han recibido confirmación por escrito de la agencia. Sin embargo, el logotipo de la FDA no puede utilizarse, ya que implica respaldo y puede conducir a responsabilidad civil o penal. Independientemente del estado de aprobación, todas las instalaciones reguladas deben cumplir con las Buenas prácticas de fabricación actuales (CGMP) y los requisitos de etiquetado.
Para los productos que requieren aprobación o autorización, como ciertos fármacos y dispositivos, la FDA también revisa y aprueba el etiquetado del producto como parte del proceso. Sin embargo, en la mayoría de los demás casos, las etiquetas no están aprobadas previamente por la FDA.
La FDA exige el cumplimiento mediante inspecciones de las instalaciones, muestreo de productos y controles de envío en la frontera.
Trabajar hacia la aprobación de la FDA con Registrar Corp
Registrar Corp ayuda a las empresas de alimentos, bebidas, fármacos, dispositivos médicos y cosméticos a navegar por las regulaciones de la FDA de los EE. UU. Ayudamos con el registro de instalaciones, la lista de productos, la revisión de etiquetas y la certificación de lotes de aditivos de color. Actuar antes de una fecha límite de cumplimiento o de una acción de cumplimiento puede evitar costosos retrasos y la pérdida de acceso al mercado.
Para obtener asistencia inmediata y asegurarse de que cumple con todos los requisitos aplicables, llame al +1-757-224-0177 o hable con un asesor regulatorio las 24 horas del día, los 7 días de la semana.



