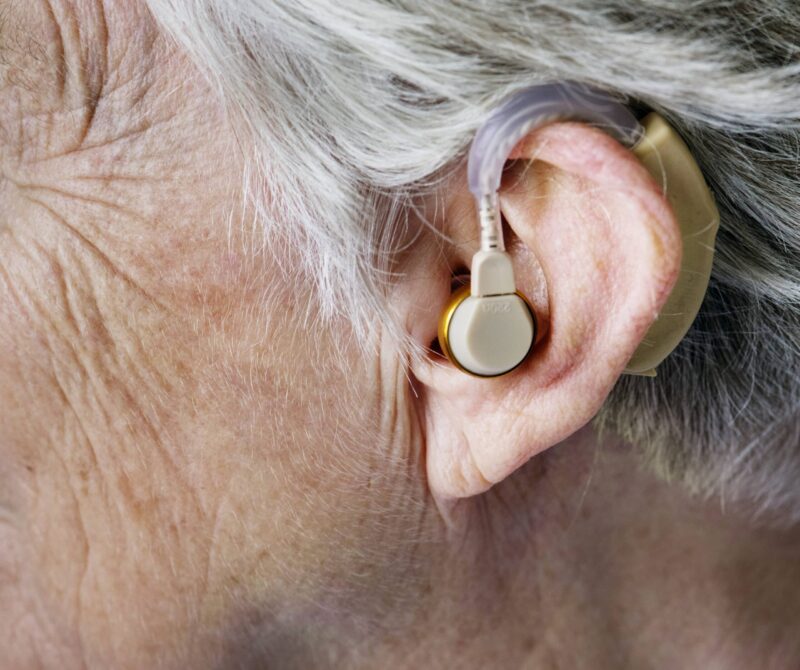
2022년 8월 17일, 미국 식품의약국(FDA)은 경증 내지 중등도의 청각 장애가 있는 소비자를 위해 새로운 일반의약품(OTC) 범주의 보청기를 확립하는 최종 규칙을 발표했습니다. 이 규칙은 2022년 10월 17일부터 소비자가 처방전, 건강 검진 또는 피팅 조정 없이 온라인 소매점 및 상점에서 보청기를 구입할 수 있도록 허용합니다. 이 조치는 미국 소비자에게 보다 저렴하고 접근 가능한 보청기 옵션을 제공하기 위한 것입니다.
OTC 보청기 제조업체의 최종 규칙 및 규정 준수 기한에 대한 배경 정보를 읽어보십시오.
FDA 규정 준수에 대한 지원을 받으십시오.
Registrar Corp의 규제 전문가는 기업이 FDA 요건을 준수하도록 지원합니다.
FDA 규제 요건에 대한 도움이 필요하시면, +1-757-224-0177번으로 전화하시거나, 이메일: 번으로 연락하시거나info@registrarcorp.com, 24시간 규제 상담사와 채팅하십시오: www.registrarcorp.com/livechat.
FDA는 바이든 대통령의 2021년 7월 미국 경제에서의 경쟁 촉진 행정 명령에 따라 2021년 10월 20일에 보청기용 OTC 약품 범주를 만들도록 제안된 규칙을
발표했습니다. 이 명령에 따라 FDA는 120일 이내에 보청기를 일반의약품으로 판매할 수 있는 조치를 취해야 했습니다. 의회는 2017년 FDA가 OTC 보청기 범주를 만들도록 요구한 유사한 법률을 통과시켰지만 당시에는 이 법률이 완전히 이행되지 않았습니다.
FDA는 이 규칙이 보청기 제조업체들 간의 혁신과 경쟁을 증가시키고 소비자들의 보청기 비용을 낮출 것으로 예상합니다. FDA는 “경증 내지 중등도의 청력 장애를 인지한 18세 이상의 사람들을 위한 특정 공기 전도 보청기”에 적용되는 규칙의 이행을 통해 OTC 보청기가 안전하고 효과적임을 보장하고자 합니다. 중증 청각 장애와 같이 규칙의 OTC 범주에 대한 요건을 충족하지 않는 보청기는 처방 의료 기기로 정의됩니다.
FDA는 과도한 볼륨으로 인한 난청을 최소화하기 위해 최대 음향 출력을 낮추는 것, 이도에 심부 보청기를 삽입하는 방법을 수정하는 것, 사용자가 조정할 수 있는 볼륨 조절을 모든 OTC 보청기에 포함하도록 요구하는 것, 소비자 이해를 돕기 위해 라벨 표현을 단순화하는 것을 포함하여 최종 규칙을 구성하기 위해 제안된 규칙의 몇 가지 변화를 포함시켰습니다.
또한 OTC 보청기 최종 규칙은 다음을 수행합니다.
- 처방 보청기에 대한 기존 규칙을 수정하여 새로운 OTC 범주와 규정을 일치시킵니다.
- 보청기 판매 조건 폐지
- 연방 OTC 보청기 규정이 주 차원의 보청기 규정에 미치는 일부 영향을 다루는 조항이 포함됩니다.
- OTC 및 처방 보청기에 대한 새로운 라벨 부착 요건을 제공합니다.
- OTC 보청기에 특정한 성능 사양 및 기기 설계 요건 포함
510(k) 허가가 있는 것을 포함하여 최종 규칙 발효일 이전에 판매용으로 제공된 OTC 보청기를 규정준수
보청기에 반입하는 것은 최종 규칙 발효일 후 180일 이내에 신규 또는 개정된 요건을 준수해야 합니다.
발효일 이전에 판매를 위해 제안되지 않았거나 판매를 위해 제안되었지만 이 규칙(§ 807.81(a)(3))과 무관한 변경으로 인해 새로운 510(k)를 제출해야 하는 보청기는 최종 규칙 발효일 또는 그 이후에 미국 시장에 진입하기 전에 새로운 또는 개정된 요건을 준수해야 합니다. 여기에는 해당하는 경우 510(k) 허가 획득이 포함됩니다.
FDA는 보청기가 다음과 같은 경우 510(k)를 제출하고 510(k) 허가를 얻기 위한 요건을 집행할 의도가 없습니다.
- 최종 규칙 발효일 이전에 합법적으로 판매를 제안받은 경우
- 규정 준수일 당일 또는 그 이전에 OTC 보청기 컨트롤을 충족하기 위한 목적으로만 510(k)의 새로운 변경이 필요한 경우
- 기기 안전성 또는 효과에 부정적인 영향을 미치지 않는 변경을 겪은 경우
- 그렇지 않으면 해당 요건을 준수합니다.
- 제조업체가 변경하고 변경 사항이 기기 안전 또는 효과에 부정적인 영향을 미치지 않는다고 판단한 준수일 또는 그 이전에 문서화한 경우
FDA 규정 준수에 대한 지원을 받으십시오.
Registrar Corp의 규제 전문가는 기업이 FDA 요건을 준수하도록 지원합니다.
FDA 규제 요건에 대한 도움이 필요하시면, +1-757-224-0177번으로 전화하시거나, 이메일: 번으로 연락하시거나info@registrarcorp.com, 24시간 규제 상담사와 채팅하십시오: www.registrarcorp.com/livechat.