Para cumplir con la fecha límite del 29 de diciembre de 2023, las compañías cosméticas se preparan para cumplir con los nuevos requisitos de la Ley de Modernización de Regulación de Cosméticos (Modernization of Cosmetics Regulation Act, MoCRA).
La FDA continúa compartiendo orientación sobre el nuevo portal de presentación electrónica, el formato de Etiquetado Estructurado de Productos (SPL) y el formato de Cosméticos Directos.
Portal directo de cosméticos
En septiembre de 2023, la FDA publicó un nuevo documento de 81 páginas, Capturas de pantalla del portal de presentación electrónica para cosméticos. Este documento proporciona el recorrido del usuario para el registro de instalaciones y la lista de productos cosméticos según lo requerido por MoCRA.
También muestra las fallas de validación que pueden ocurrir al enviar su información.
La FDA ha hecho un trabajo fantástico educando a la industria sobre qué esperar de MoCRA. Esta vista previa ayuda a las empresas a determinar si son capaces de manejar las presentaciones del portal o si necesitarán experiencia externa.
La FDA comenzó a aceptar comentarios sobre el nuevo borrador del portal de presentación electrónica (Cosmetics Direct) y los formularios impresos. La fecha límite para enviar un comentario fue el 18 de octubre de 2023.
Un vistazo al formato de etiquetado estructurado de productos (SPL)
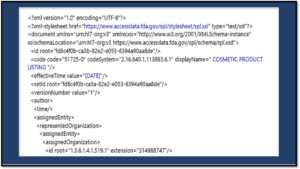
El nuevo portal Cosmetics Direct destaca el formato SPL, un componente clave del software estructurado de etiquetado de productos, que se requerirá para todas las presentaciones de cosméticos. Para aquellas compañías de cosméticos donde el formato SPL es un territorio nuevo, los ejemplos, el formato XML y la validación pueden parecer complicados.
Antes de que se publicaran las capturas de pantalla, la única información disponible para la industria estaba en la Guía preliminar para la industria. Esta guía indicaba que usted debía enviar los datos de registro y listado en el formato SPL y proporcionaba estos detalles:
“El registro de las instalaciones de productos cosméticos y la lista de productos estarán disponibles utilizando el mismo proceso de presentación electrónica disponible para registrar un establecimiento y enumerar un fármaco con la FDA. Esto ayudará a agilizar el proceso de envío de información de registro y listado para instalaciones y productos cosméticos para entidades que también envían información de establecimiento y listado de medicamentos”.
Guía de implementación y procedimientos de validación de SPL
En octubre, la FDA publicó una guía para la implementación y validación de SPL. La guía de 275 páginas describe a Cosmetics Direct como una herramienta de creación de SPL fácil de usar que realizará validaciones iniciales, creará y guardará presentaciones de SPL y las enviará a la FDA.
El 14 de noviembre, la FDA actualizó la Guía de implementación de SPL para incluir actualizaciones adicionales a los registros de las instalaciones de productos cosméticos y los listados de productos incluidos en el marco de SPL.
Próximas fechas límite de cumplimiento de MoCRA
La FDA aún no ha anunciado la fecha exacta de lanzamiento del portal de presentación de Cosmetics Direct. Pero se lanzará a tiempo para que las instalaciones cumplan con la próxima fecha límite del 29 de diciembre de 2023.
La FDA anunció una fecha de cumplimiento demorado del 1 de julio de 2024 o seis meses después de la fecha límite del 29 de diciembre. Esta actualización reconoce las complejidades de las presentaciones de SPL y brinda a las instalaciones de cosméticos tiempo adicional para cumplir con los requisitos.
La extensión se aplica a las instalaciones de cosméticos que comenzaron a fabricar o procesar productos cosméticos después del 29 de diciembre de 2022. En lugar de tener que registrarse antes de la fecha límite de diciembre, solo tendrán que completar la inscripción antes del 1 de julio.
Las compañías que comenzaron a comercializar productos cosméticos después del 29 de diciembre de 2022 también tendrán seis meses adicionales antes de que la FDA haga cumplir los requisitos de cotización de MoCRA.
Registrar Corp puede ayudar
Con la amplia experiencia de Registrar Corp en la presentación de listas de medicamentos de la FDA en formato SPL, las compañías de cosméticos confían en que Registrar Corp se asegurará de cumplir con los nuevos requisitos cosméticos de la FDA en virtud de la MoCRA y les ayudará con las presentaciones de Cosmetics Direct.
Vea todo el documento con una vista previa del nuevo portal de cosméticos y descubra lo que Registrar Corp puede hacer por su empresa para cumplir con las nuevas regulaciones.