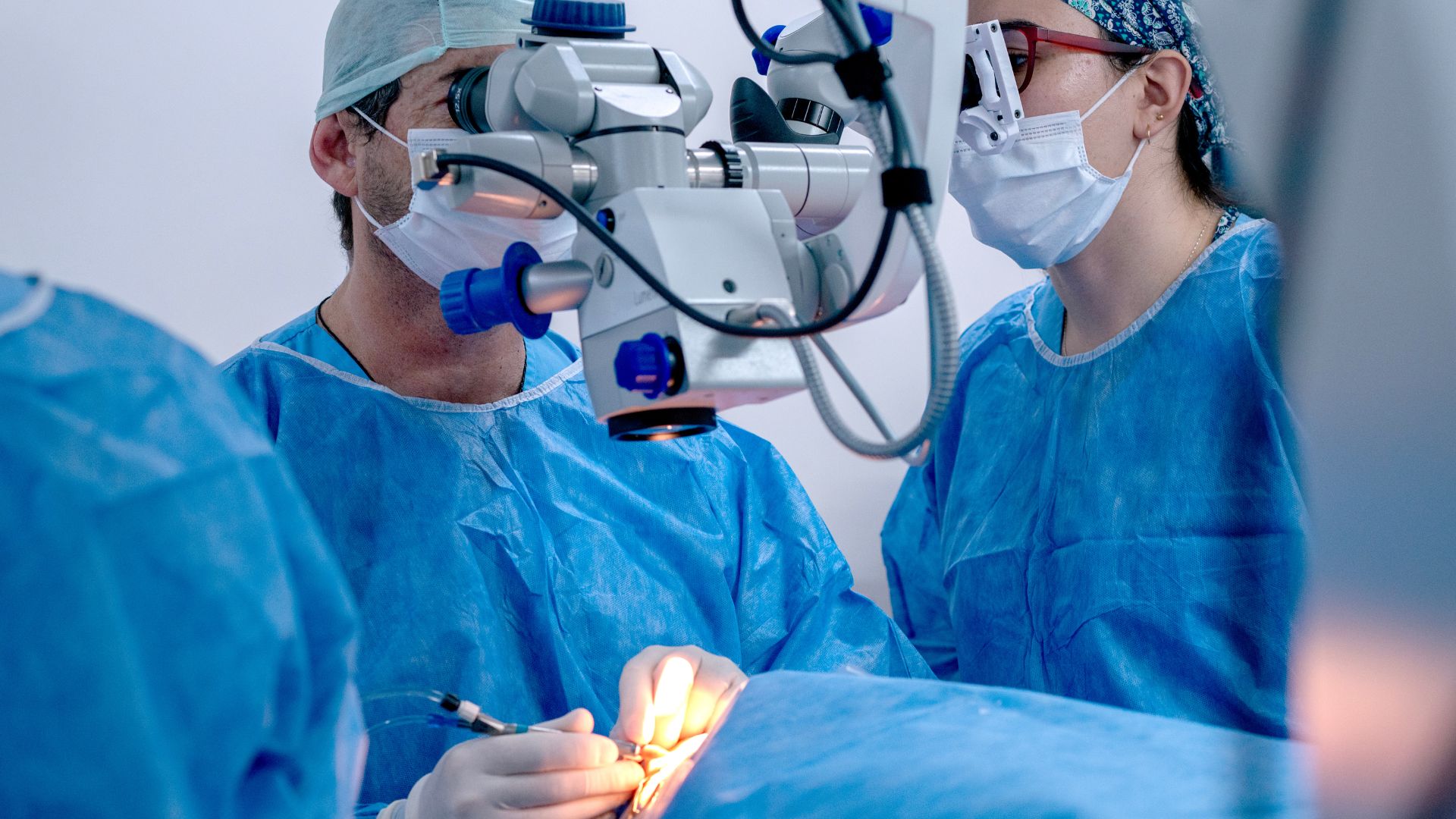
Gli strumenti e i dispositivi chirurgici oftalmologici, compresi bisturi, pinze, sistemi di facoemulsificazione e strumenti chirurgici laser-assistiti, svolgono un ruolo fondamentale nella correzione della vista e nel trattamento delle malattie oculari. A causa della loro natura invasiva e dell’impatto diretto sugli esiti dei pazienti, questi prodotti sono soggetti a una stretta supervisione della FDA. I produttori devono classificare correttamente i propri dispositivi, rispettare le normative pre-commercializzazione e post-commercializzazione e soddisfare gli standard UDI ed etichettatura per evitare avvisi di importazione, arresti e ritardi normativi.
Come la FDA classifica i dispositivi chirurgici oftalmici
La FDA assegna strumenti chirurgici oftalmici a diverse categorie basate sul rischio:
- Classe I (basso rischio): Include strumenti manuali come bisturi e pinze. Questi sono spesso esenti da autorizzazione 510(k) ma richiedono ancora la registrazione dell’istituzione e l’elenco dei dispositivi medici.
- Classe II (rischio moderato): Include sistemi di facoemulsificazione, laser chirurgici e dispositivi di iniezione intraoculare. Questi richiedono una clearance di 510(k) per dimostrare una sostanziale equivalenza.
- Classe III (alto rischio): Copre dispositivi impiantabili come lenti intraoculari (IOL) e cornee artificiali. Questi richiedono l’approvazione pre-commercializzazione (PMA) con un’ampia convalida clinica.
Passi per commercializzare legalmente i dispositivi chirurgici oftalmici negli Stati Uniti
I produttori devono completare i seguenti passaggi:
- Registrazione dell’istituto: Richiesto annualmente per tutti i produttori e importatori.
- Elenco dei dispositivi medici: Ciascun dispositivo chirurgico deve essere elencato sotto la sede legale.
- Conformità UDI: La maggior parte degli strumenti chirurgici oftalmici richiede identificatori univoci del dispositivo per la tracciabilità e la preparazione al richiamo.
- Conformità in materia di etichettatura e pubblicità: Un’etichettatura fuorviante o incompleta può innescare arresti e richiami delle importazioni.
Sfide e soluzioni comuni per la conformità
Comprendere questi scenari reali può aiutare i produttori a evitare ritardi:
Caso di studio: Sistema di facoemulsificazione ritardato a causa di UDI mancante
Un produttore ha tentato di importare un sistema chirurgico senza etichettatura conforme all’UDI. Ciò ha comportato:
- Lancio ritardato del prodotto durante l’aggiornamento dei dati di imballaggio e conformità.
- Costi aggiuntivi per la rietichettatura e la ripresentazione dell’elenco dei dispositivi.
- Consulenza normativa per correggere i processi interni.
Caso di studio: Dispositivo laser oftalmico classificato erroneamente
Una società ha classificato erroneamente un laser per chirurgia refrattiva come Classe II. Dopo la revisione della FDA, è stato riclassificato come Classe III, richiedendo PMA:
- L’approvazione è stata ritardata da ampi requisiti di test clinici.
- I costi sono aumentati a causa della necessità di ulteriori dati di sicurezza ed efficacia.
- È stata presentata una richiesta 513(g) per chiarire la classificazione per i prodotti futuri.
Considerazioni normative per i produttori
- Commissioni utente FDA: Richiesto annualmente; potrebbe essere disponibile l’assistenza per le tariffe per le piccole imprese.
- Avvisi di importazione: Le spedizioni non conformi possono essere trattenute automaticamente.
- Certificato per il governo straniero (CFG): Spesso necessario per l’esportazione.
- Licenza Health Canada: Un MDEL può essere richiesto per le vendite canadesi.
Mantenere la conformità dopo l’ingresso sul mercato
I produttori devono mantenere la conformità per molto tempo dopo il lancio del prodotto:
- Segnalazione eMDR: Gli eventi avversi devono essere segnalati alla FDA.
- Richieste FOIA: Aiuta a confrontare le approvazioni dei dispositivi simili.
- File master dispositivo medico: Supporta l’invio di componenti proprietari.
- Consulenza normativa in corso: Garantisce l’allineamento con le aspettative FDA in evoluzione.
Creazione di un percorso normativo chiaro per i dispositivi oftalmici
Portare con successo i dispositivi chirurgici oftalmici sul mercato statunitense richiede più dell’approvazione normativa. Una classificazione accurata, la conformità UDI, l’etichettatura convalidata e la vigilanza post-commercializzazione sono essenziali. Affrontando in modo proattivo i requisiti della FDA, i produttori possono ridurre al minimo i ritardi, evitare azioni di applicazione e garantire il successo a lungo termine nel mercato competitivo dei dispositivi chirurgici.